
Энтерит у щенка 3 мес — советы врачей на каждый день
Парвовирусный энтерит — высококонтагиозное и быстропротекающее инфекционное заболевание собак, часто приводящее к смертельному исходу. Возникло оно сравнительно недавно, в 1978 году в Северной Америке и […]

Шумит в голове — советы врачей на каждый день
Шум в голове – неприятный симптом, возникающий на фоне различных заболеваний. Он может проявляться свистом, шипением или звоном. Звуки могут проявляться периодически или беспокоят человека […]
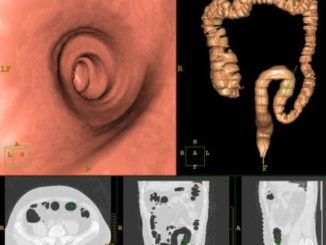
Что показывает КТ кишечника? — советы врачей на каждый день
КТ кишечника в клиниках СПб применяется для исследования толстого и тонкого кишечника, желудка, лимфатических узлов, соседних сосудов путем их сканирования с помощью рентгеновских лучей. В […]

Что означают фразы мужчин? — советы врачей на каждый день
В заботе о своем здоровье нет ничего сложного. Достаточно соблюдать несколько правил, чтобы довольно быстро увидеть положительные результаты. Причем правила эти просты, логичны и выполнение […]

Что делать,если не стоит пеннис — советы врачей на каждый день
Развитие медицины в настоящее время идет по многим направлениям, в том числе наука не обходит стороной такую важную проблему, как плохая эрекция или ее отсутствие […]